20 de maio - Dia nacional do medicamento genérico
Data de publicação: 20 de maio de 2024
Os medicamentos genéricos foram instituídos no Brasil com a promulgação da Lei 9787/1999, que teve como objetivo ampliar o acesso da população a medicamentos.
Para ser aprovado, o genérico deve apresentar mesma forma farmacêutica, via de administração e quantidade de substância ativa que o medicamento a que está sendo comparado e demonstrar que a quantidade absorvida e a velocidade de absorção são comparáveis.
Substituição por genérico
O farmacêutico está autorizado a substituir o medicamento prescrito pelo genérico correspondente.
Para isso, deve indicar a substituição na prescrição e incluir as seguintes informações:
- Apor seu carimbo, com nome e número de inscrição no CRF;
- Colocar a data;
- Assinar.
Substituição não autorizada
Caso o prescritor não autorize a substituição, deverá manifestar sua vontade da seguinte forma:
- Escrito à mão, em cada item;
- De forma clara, legível e inequívoca;
- Não é permitido manifestar-se de forma impressa.
Intercambialidade entre medicamentos*
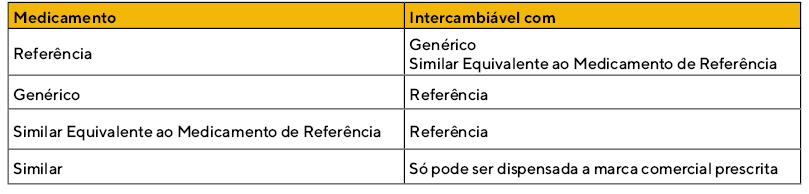
*A substituição deve ser realizada de acordo com as listas publicadas pela Anvisa.
Referências
BRASIL. Agência Nacional de Vigilância Sanitária. Conceitos e definições. Disponível em: <www.gov.br/anvisa/pt-br/acessoainformacao/perguntasfrequentes/medicamentos/conceitos-e-definicoes>. Acesso em 20 mai. 2024.
BRASIL. Agência Nacional de Vigilância Sanitária. Resolução RDC no 16, de 2 de março de 2007. Aprova o regulamento técnico para medicamentos genéricos, Anexo I. Acompanha esse regulamento o Anexo II, intitulado “Folha de rosto do processo de registro e pós-registro de medicamentos genéricos”. Diário Oficial da União, Brasília, 5 mar. 2007.
BRASIL. Agência Nacional de Vigilância Sanitária. Resolução RDC nº 58, de 10 de outubro de 2014. Dispõe sobre as medidas a serem adotadas junto à Anvisa pelos titulares de registros de medicamentos para a intercambialidade de medicamentos similares com o medicamento de referência. Diário Oficial da União, Brasília, 13 out. 2014.
BRASIL. Lei no 9787, de 10 de fevereiro de 1999. Altera a Lei no 6.360, de 23 de setembro de 1976, que dispõe sobre a vigilância sanitária, estabelece o medicamento genérico, dispõe sobre a utilização de nomes genéricos em produtos farmacêuticos e dá outras providências. Diário Oficial da União, Brasília, 11 fev. 1999.
>> Saiba mais sobre intercambialidade de medicamentos no Boletim do CIM 3/2022